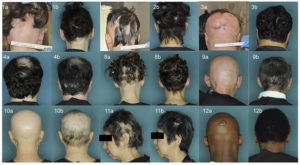
Approvato nuovo farmaco contro l’alopecia areata. La FDA approva LITFULO™ (Ritlecitinib) di Pfizer per adulti e adolescenti con grave alopecia areata
LITFULO è il primo e unico trattamento per l’alopecia areata grave approvato per pazienti a partire dai 12 anni di età.
L’annuncio
NEW YORK, 23 giugno 2023. Pfizer Inc. ha annunciato oggi che la Food and Drug Administration (FDA) statunitense ha approvato LITFULO™ (Ritlecitinib), un trattamento orale da assumere una volta al giorno, per i soggetti di età pari o superiore a 12 anni affetti da alopecia areata grave. La dose raccomandata approvata per LITFULO è di 50 mg. Si tratta peraltro del primo e unico trattamento approvato dalla FDA per gli adolescenti (12+) con alopecia areata grave.
“Sebbene i pazienti possano iniziare a sviluppare i sintomi dell’alopecia areata a qualsiasi età, la maggior parte delle persone inizia a manifestare i primi sintomi verso l’adolescenza, i vent’anni o i trenta”, ha dichiarato la dottoressa Brittany Craiglow, Professore Associato Aggiunto di Dermatologia presso la Yale School of Medicine. “LITFULO è un’opzione terapeutica particolarmente importante per i pazienti più giovani con una forte perdita di capelli, che spesso lottano con una malattia così visibile”.

LITFULO è il primo farmaco approvato per le forme di alopeica areata grave.
LITFULO è un inibitore della chinasi, per la precisione inibisce la Janus chinasi 3 (JAK3) e la famiglia delle tirosine chinasi espresse nel carcinoma epatocellulare (TEC).
“LITFULO rappresenta un importante progresso terapeutico per l’alopecia areata, una malattia autoimmune che in precedenza non aveva opzioni approvate dalla FDA per gli adolescenti e limitate per gli adulti”, ha dichiarato Angela Hwang, Chief Commercial Officer, President, Global Biopharmaceuticals Business, Pfizer. “Con l’approvazione odierna, gli adolescenti e gli adulti che lottano contro una consistente perdita di capelli hanno l’opportunità di ottenere una significativa ricrescita dei capelli sul cuoio capelluto”.
L’approvazione della FDA si basa sui risultati degli studi clinici condotti sull’alopecia areata. Lo studio ALLEGRO di Fase 2b/3, che ha arruolato 718 pazienti con una perdita di capelli sul cuoio capelluto pari o superiore al 50%, misurata dal Severity of Alopecia Tool (SALT), ha valutato l’efficacia e la sicurezza di LITFULO in 118 siti in 18 Paesi.
Lo studio
In questo studio di base, il 23% dei pazienti trattati con LITFULO 50 mg ha ottenuto una copertura dei capelli del cuoio capelluto pari o superiore all’80% (SALT≤20) dopo sei mesi, rispetto all’1,6% con placebo. L’efficacia e la sicurezza di LITFULO sono risultate coerenti tra gli adolescenti (dai 12 ai 17 anni) e gli adulti (dai 18 anni in su). Gli eventi avversi più comuni riportati in almeno il 4% dei pazienti con LITFULO includono cefalea (10,8%), diarrea (10%), acne (6,2%), rash (5,4%) e orticaria (4,6%). I risultati completi dello studio di Fase 2b/3 di ALLEGRO sono stati pubblicati da The Lancet nell’Aprile 2023.
“Le persone che vivono con l’alopecia areata spesso non sono comprese e la loro esperienza viene sovente banalizzata come “si tratta solo di capelli”. Si tratta invece di una grave malattia autoimmune che può avere un notevole impatto negativo al di là dei sintomi fisici”, ha dichiarato Nicole Friedland, Presidente e Amministratore Delegato della National Alopecia Areata Foundation (NAAF). “Riteniamo che l’approvazione di LITFULO rappresenti un progresso significativo per il trattamento dell’alopecia areata, in particolare per gli adolescenti. È entusiasmante vedere che altri trattamenti approvati dalla FDA diventano disponibili per questa comunità”.
LITFULO sarà disponibile nelle prossime settimane.
Risultati ottenuti con il farmaco Roxolitinib, analgo a LITFULO.
Informazioni sull’alopecia areata
L’alopecia areata è una malattia autoimmune caratterizzata da una perdita di capelli, a chiazze o completa, sul cuoio capelluto, sul viso o sul corpo. Ha una patogenesi immuno-infiammatoria sottostante e si sviluppa quando il sistema immunitario attacca i follicoli piliferi dell’organismo, causando la caduta dei capelli e dei peli del corpo. La perdita di capelli si verifica spesso, ma la perdita può interessare anche le sopracciglia, le ciglia, i peli del viso e altre aree del corpo. L’alopecia totalis (perdita totale dei capelli) e l’alopecia universalis (perdita totale dei capelli e dei peli del corpo) sono tipi di alopecia areata.
L’alopecia areata, che colpisce quasi 7 milioni di persone negli Stati Uniti e circa 147 milioni di persone in tutto il mondo, può colpire persone di qualsiasi età, sesso, razza o etnia e può arrecare un danno considerevole oltre alla perdita di capelli. Quasi il 20% delle alopecie areate viene diagnosticato prima dei 18 anni.
Alopecia areata. Il programma di sperimentazione clinica
Lo studio randomizzato, controllato con placebo e in doppio cieco ALLEGRO di Fase 2b/3 ha studiato LITFULO in pazienti di età pari o superiore a 12 anni con alopecia areata. I pazienti inclusi nello studio presentavano una perdita di capelli pari o superiore al 50%, come misurato dal Severity of Alopecia Tool (SALT), compresi i pazienti con alopecia totalis e alopecia universalis, che stavano vivendo un episodio di alopecia areata che durava da sei mesi a 10 anni.
I pazienti sono stati randomizzati a ricevere LITFULO una volta al giorno (50 mg, 30 mg, 10 mg) con o senza un mese di trattamento iniziale con LITFULO 200 mg una volta al giorno, oppure a ricevere placebo una volta al giorno per 24 settimane. Alla settimana 24, i gruppi LITFULO hanno continuato le dosi assegnate e i pazienti inizialmente assegnati al placebo sono passati a LITFULO (50 mg o 200 mg dose di carico + 50 mg) per altre 24 settimane.

La grande casa farmaceutica Pfizer ha realizzato in tempi piuttosto brevi questo farmaco efficace contro l’areata.
In questo studio di base, una percentuale statisticamente significativa di pazienti trattati con LITFULO 50 mg ha raggiunto una copertura dei capelli pari o superiore all’80% (SALT≤20) dopo sei mesi di trattamento rispetto al placebo (23% trattati con LITFULO 50 mg rispetto all’1,6% con placebo).
Gli effetti indesiderati più comuni che si sono verificati in almeno l’1% dei pazienti nelle 24 settimane sono stati: cefalea, diarrea, acne, rash cutaneo, orticaria, follicolite, piressia, dermatite atopica, vertigini, aumento della creatinina fosfochinasi nel sangue, herpes zoster, riduzione della conta dei globuli rossi e stomatite. Sono stati riportati anche casi di infezioni gravi, tumori maligni, eventi tromboembolici e anomalie di laboratorio.
Ulteriori informazioni sullo studio di Fase 2b/3 di ALLEGRO sono disponibili sul sito https://www.clinicaltrials.gov.
ALLEGRO-LT è uno studio di Fase 3, in aperto, a lungo termine, per studiare la sicurezza e l’efficacia di LITFULO negli adulti con alopecia areata con perdita di capelli del 25% o superiore e negli adolescenti a partire dai 12 anni di età con alopecia areata con perdita di capelli del 50% o superiore.
Informazioni su LITFULO™ (Ritlecitinib)
LITFULO è un inibitore di JAK3 e delle chinasi della famiglia TEC. L’inibizione di JAK3 e dei membri della famiglia TEC chinasi da parte di LITFULO può bloccare la segnalazione di citochine e l’attività citolitica dei linfociti T, che è implicata nella patogenesi dell’alopecia areata.
Le domande di autorizzazione per LITFULO nell’alopecia areata sono state sottoposte all’esame di Paesi di tutto il mondo, tra cui Cina, Unione Europea, Giappone e Regno Unito. L’Agenzia Europea per i Medicinali (EMA) ha accettato la domanda di autorizzazione all’immissione in commercio (MAA) per Ritlecitinib e la decisione è prevista per il terzo trimestre del 2023.
LITFULO è in fase di valutazione anche per la vitiligine, la malattia di Crohn e la colite ulcerosa.
La cefalea è il principale effetto collaterale di questo farmaco.
Indicazioni
LITFULO è un inibitore della chinasi indicato per il trattamento dell’alopecia areata grave negli adulti e negli adolescenti a partire dai 12 anni.
Limitazioni d’uso: Non è raccomandato l’uso in combinazione con altri inibitori della JAK, immunomodulatori biologici, ciclosporina o altri potenti immunosoppressori.
Informazioni importanti sulla sicurezza
LITFULO può causare gravi effetti collaterali, tra cui:
Infezioni gravi. LITFULO può ridurre la capacità del sistema immunitario di combattere le infezioni. Non iniziate a prendere LITFULO se avete qualsiasi tipo di infezione, a meno che il vostro medico non vi dica che va bene. Alcune persone hanno avuto gravi infezioni durante l’assunzione di LITFULO o di altri farmaci simili, tra cui tubercolosi (TBC) e infezioni causate da batteri, funghi o virus che possono diffondersi in tutto il corpo, e sono state ricoverate in ospedale. Alcune persone che assumono farmaci simili a LITFULO sono morte a causa di queste infezioni. Il rischio di sviluppare l’herpes zoster è più elevato.
Prima di iniziare il trattamento con LITFULO, il medico deve sottoporla a un test per la tubercolosi e deve osservarla attentamente per individuare eventuali segni e sintomi di tubercolosi durante il trattamento con LITFULO.
Prima e dopo l’inizio del trattamento con LITFULO, informi subito il medico se ha un’infezione, se è in trattamento per un’infezione o se presenta i sintomi di un’infezione, tra cui: febbre, sudorazione o brividi, dolori muscolari, tosse o respiro corto, sangue nel catarro, perdita di peso, pelle calda, rossa o dolorosa o piaghe sul corpo, diarrea o dolore allo stomaco, bruciore durante la minzione o minzione più frequente del solito, sensazione di grande stanchezza.
LITFULO può aumentare la probabilità di contrarre infezioni o peggiorare le infezioni già presenti. In caso di infezione grave, il medico può interrompere il trattamento con LITFULO fino a quando l’infezione non sarà controllata.

Con l’approvazione dell’EMA l’Agenzie Europea del Farmaco, LITFULO sarà probabilmente disponibile nella EU alla fine del 2023.
Esiste un aumento del rischio di morte nelle persone di 50 anni e più che hanno almeno un fattore di rischio di malattia cardiaca (cardiovascolare) e che assumono un inibitore della Janus chinasi (JAK). LITFULO è un inibitore dei questa chinasi.
Cancro e problemi del sistema immunitario. LITFULO può aumentare il rischio di alcuni tumori modificando il funzionamento del sistema immunitario. Possono insorgere linfomi e altri tumori, compresi quelli della pelle. Le persone, in particolare i fumatori, anche ex, hanno un rischio maggiore per alcuni tumori, tra cui il linfoma e i tumori polmonari, quando assumono un inibitore della JAK. Seguire i consigli del medico in merito al controllo della pelle per verificare la presenza di tumori cutanei durante il trattamento. Informare il medico se si è mai avuto un qualsiasi tipo di cancro.
Esiste un aumento del rischio di eventi cardiovascolari maggiori, come infarto, ictus o morte, nelle persone di 50 anni e più che presentano almeno un fattore di rischio per le malattie cardiache (cardiovascolari) e che assumono un inibitore della JAK, soprattutto se fumatori attuali o ex.
Articolo tratto, tradotto e adattato da www.businesswire.com
PRODOTTI CORRELATI
Kmax healing hair transplant post-surgery follicle activator supplement è un integratore alimentare post-trapianto che incrementa la ricrescita dei capelli.
Scopri il trattamento in fiale a base di olii essenziali di lavanda, camomilla blu, tea tree oil, rosmarino, eucalipto, arnica e ippocastano per contrastare la caduta di capelli di diverse natura. Ideale anche come preparazione al trapianto di capelli
APPROFONDIMENTI